خطر زئونوزی (بیماری قابل انتقال از حیوان به انسان):
یک دلیل خوب دیگر که چرا باید گربه ها را از خفاش ها دور نگه داشت
ترجمه: دکتر سید شهرام میرزمانی
معاون بهداشت اداره بهداشت امداد و درمان نیروی دریایی راهبردی
DVM-MPH- Ph.D. Candidate in Microbiology
Islamic Azad University, Science and Research Branch
ss.mirzamani@gmail.com
خلاصه
خفاش ها اغلب به طور ناعادلانه به عنوان مقصر مستقیم در همه گیر کنونی کووید-19 به تصویر کشیده می شوند، اما علل واقعی این و سایر رویدادهای سرریززئونوزی را باید در تأثیر انسان بر محیط زیست، از جمله گسترش حیوانات اهلی جستجو کرد.
در این مقاله، محققاندرباره شکار خفاش توسط گربه ها به عنوان پدیده ای که خطرات زئونوزی را به وجود می آورد، بحث کردند و موارد انتقال، مشاهده، مشکوک یا فرضیه انتقال پاتوژن از خفاش به گربه ، قطعاً یا به احتمال زیاد پس از دوره های شکاررا نشان می دهند. علاوه بر موارد شناخته شده هاری خفاش، محققان بیماری های دیگری را که انسان به آنها مبتلا می شوند، مرور می کنندکه در نهایت ممکن است از طریق گربه هایی که خفاش ها را شکار می کنند، به انسان برسد. محققان همچنین انتقال بالقوه سارس-کووی-2، عامل ایجاد کننده بیماری کووید-19، از گربه های خانگی به خفاش ها را بررسی می کنند، که اگرچه بعید به نظر می رسد، ممکن است یک مخزن حیات وحش جدید در این پستانداران ایجاد کند، و جهت گیری تحقیق و مدیریت را برای دستیابی ارزیابی خطر، کاهش اثریا پیشگیری موثرتررا شناسایی کنند.به طور کلی، نه تنها کشتن خفاش توسط گربه ها تهدیدی جدی برای حفاظت از تنوع زیستی است، بلکه دارای پیامدهای زئونوزی است که دیگر نمی توان از آنها غافل شد.
واژگان کلیدی: خفاش؛ گربه؛ گربه های اهلی؛ کووید -19؛ سارس-کووی-2،پسزدگی یا بازگشت به عقب (spillback)؛ سرریز (spillback)؛ خطر زئونوزی؛ استراتژی سلامت واحد؛
منبع اصلی:
Salinas-Ramos, V.B.; Mori, E.; Bosso, L.; Ancillotto, L.; Russo, D. Zoonotic Risk: One More Good Reason Why Cats Should Be Kept Away from Bats. Pathogens 2021, 10, 304.https://doi.org/10.3390/ pathogens10030304
1. مقدمه
پیشرفت پاندمی کووید -19 (بیماری کروناویروس 2019) نقش اصلی حیات وحش را در رویدادهای زئونوزی برجسته کرده است (برای مثال [1]) که به دلیل تراکم و تحرک بالای جمعیت انسانی می تواند به سرعت در مناطق وسیع جهان گسترش یابد. در حالی که بیشتر توجه عموم مردم معطوف به اپیدمیولوژی سارس-کووی-2 به عنوان یک عامل بیماری زای انسانی است، اما تردید کمی وجود دارد که در عوامل علیتی ناشی از سرریز مستقیم یا غیرمستقیم از جمله مصرف خفاش ها توسط انسان اغلب در آسیا نهفته است [2]. به طور کلی، در مورد این واقعیت اتفاق نظر وجود دارد که بیماریهای زئونوزی به دلیلرشد مداوم جنگل زدایی و گسترش مناطق زراعی و شهریبا هزینه زیستگاه های طبیعی، افزایش فرصت هایکنش های متقابل حیات وحش - انسان، و همچنین تجارت و مصرف حیات وحش به شدت مورد علاقه است [3]. بنابراین واضح است که برای جلوگیری از فرایندهای سرریز و رویدادهای پاندمی آینده، اتخاذ یک رویکرد جامع برای پیشگیری از بیماری های زئونوز با در نظر گرفتن پویایی های اجتماعی- اکولوژیکی انسان، حیات وحش و محیط زیست ضروری است.
خطر زئونوزی در ارتباط با حیات وحش اغلب چند وجهی است و ممکن است چندین بازیگر را درگیرنماید. بنابراین، فقط مراقبت دقیق بر روی همه گونه هایی که در شبکه کنش متقابل انسان - حیات وحش شرکت می کنند، می تواند منجر به جلوگیری و کاهش اثر موثر شود. حیوانات اهلی ممکن است در پل زدن حیات وحش و انسان ها در موقعیت هایی که بطور دیگر تماس مستقیم انسان - حیوان وحشی نادر است، یک نقش حیاتی زئونوزی داشته باشند، که تقویت کننده پاتوژن یا به عنوان یک مخزن برای تنوع ژنتیکی عمل نماید [4]. برای مثال، در مورد ویروس نیپا در مالزی، خوک های اهلی به عنوان تقویت کنندهاین ویروس خفاش های میوه خوار عمل کرده و آن را به انسان منتقل می نمایند [5].
خفاش ها اغلب به عنوان گونه هایی شناخته می شوند که دارایطرفیت زئونوزی هستند ([6]؛ اما به [7] مراجعه نمائید) و مخازن طبیعی عوامل بیماری زا (به ویژه ویروس ها) که ممکن است انسان ها را مستقیماًیاپس از یک مسیر پیچیده تر که شامل سایر گونه های جانوری می شود، آلوده نمایند. در حالی که خطرات ناشی از خفاش ها توسط خدمات حیاتی اکوسیستم این پستانداران را تحت فشار قرار می گیرد، و بیان نادرست چنین خطرات زئونوزی ممکن است به حفاظت از خفاش آسیب برساند [8]، یک استدلال که اغلب نادیده گرفته می شود این است که تماس مستقیم بین خفاش ها و مردم در صورت استفاده از گوشت شکار و تجاوز انسان به زیستگاه خفاش نسبتاً بعید است. خفاش ها پستانداران شب گرد و گریزانهستند که به طور معمول از تماس با انسان هاخودداری می کنند و بهت عرض های انسانی بسیار حساس هستند، چنین تماس هایی در واقع بسیار نادر است. با این حال، شکار خفاش ها توسط حیوانات اهلی که تماس مکرر با انسان دارند، ممکن است یک پیوند مهم اپیدمیولوژیکی باشد که تاکنون فقط بخشی از آن کشف شده است.
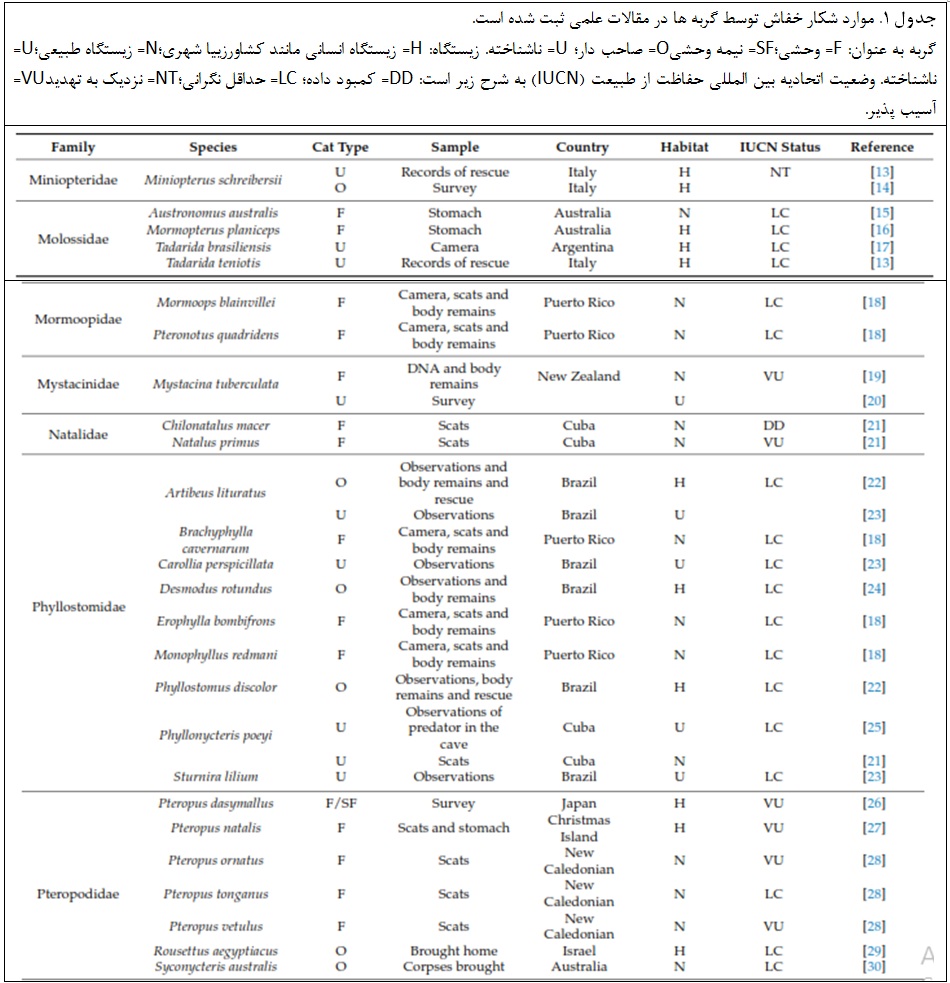
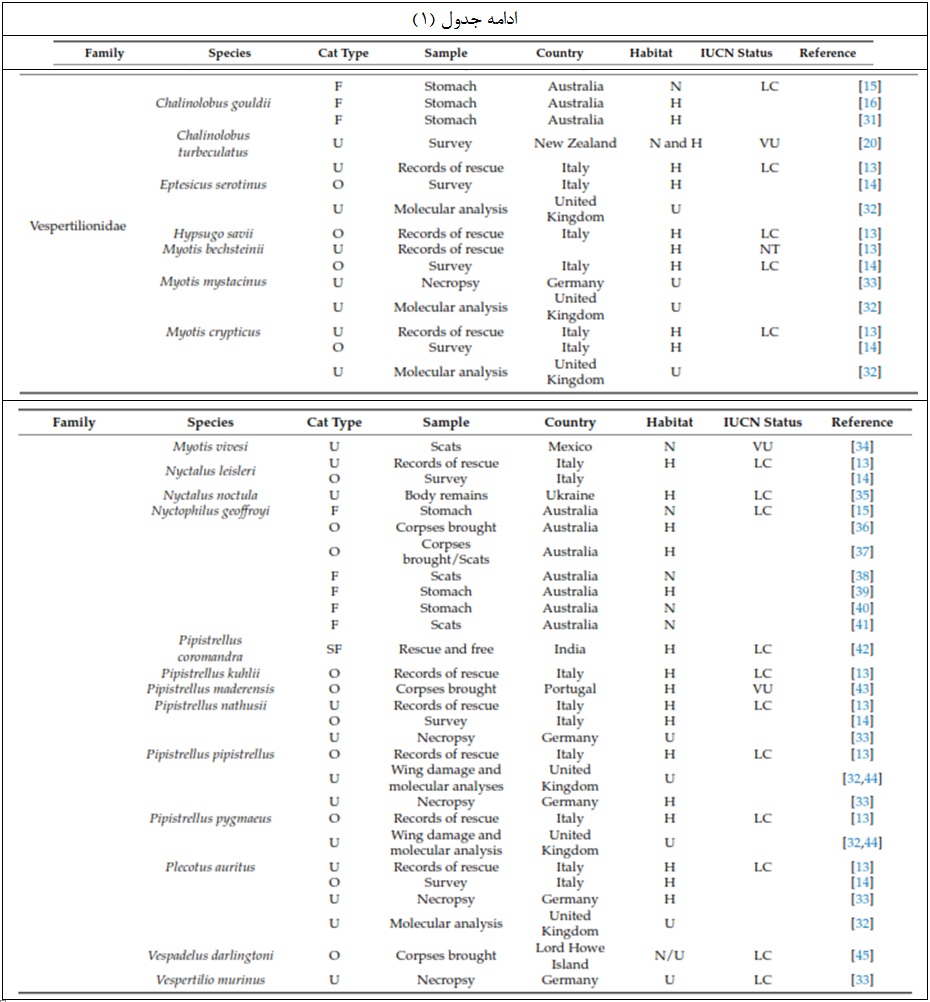
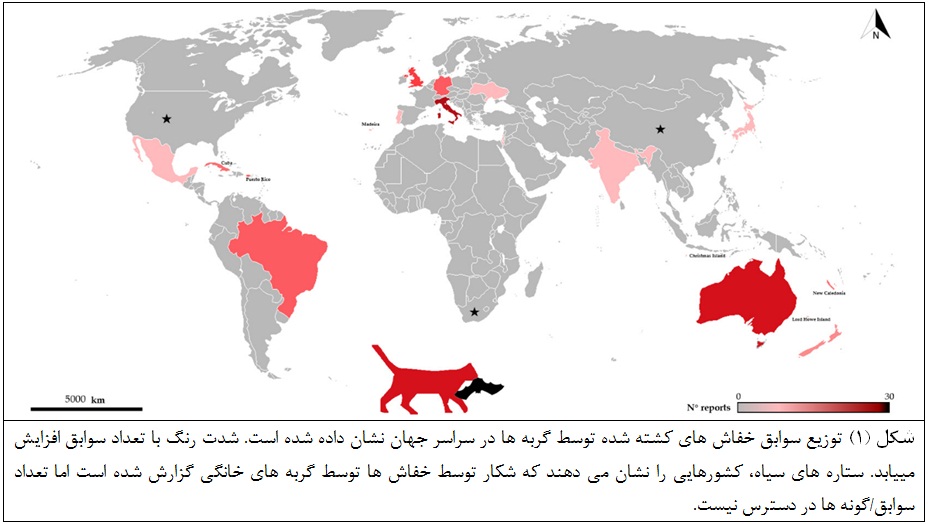
همانطور که در سراسر جهان ثبت شده، گربه های اهلی شکارچیان شناخته شده بسیاری از گونه های حیات وحش هستند [9]، گاهی اوقات در نظام های اکولوژیکی آسیب پذیر مانند جزایر [10] ممکن است تأثیر آنها به ویژه برجسته باشد. در مورد خفاش ها، موارد شکار توسط گربه های اهلی 48 گونه خفاش و 20 کشور را پوشش می دهد(به شکل 1 و جدول 1نگاه کنید)، و با توجه به مشکلات موجود در ثبت چنین رویدادهایی، شکی نیست که این پدیده بسیار گسترده تر از آنچه قبلا به تصور کشیده شده است.
برای مثال، مشخص شد که شکار گربه اولین دلیل ورود به مراکز نجات حیات وحش ایتالیا برای خفاش هایبالغ است [13].
در حالی که اثرات جمعیتیواقعی شکار گربهبر حیات وحش ناشناخته است، اما به نظر می رسد مهم است، به طور کلی تردیدکمی وجود دارد که در آنجا که خفاش ها و گربه هایاهلی به طور مشترک حضور دارند، این امر بطور معمول دردوره های شکار اتفاق می افتد (به جدول 1و منابع موجود در آن مراجعه نمائید). این موضوع اغلب از نظر عواقب حفاظتی مورد بحث قرار می گیرد زیرا بسیاری از گونه های خفاش در معرض خطر هستند و شکار گربه ممکن است حداقل با سایر تهدیدها که منجر به به خطر انداختن وضعیت حفاظت از خفاش می شوند، هم افزایی داشته باشند، به ویژه هنگامی که جمعیت خفاش های کوچک در حال کاهش است، درگیر می شوند.
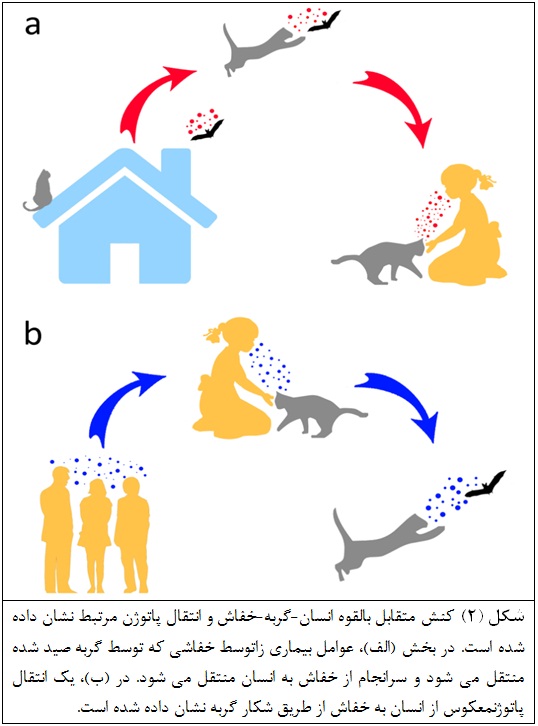
به طور کلی، پاتوژن های اجباری زئونوزی معمولاً از یک حیوان به افراد منتقل می شوند (در این صورت، انسان به طور معمول عامل بیماری زا را از حیوانات دریافت می کنند). از طرف دیگر، عوامل بیماری زای انسانی به طور معمول از انسانی به انسان دیگر منتقل می شوند، اما در صورت داشتن مخزن حیوانات، ممکن است از حیوان به فرد نیز منتقل شوند. سرانجام، یک پاتوژن حیوانی ممکن است تکامل یافته و با گونه های ما سازگار شود و به یک پاتوژن انسانی جدید تبدیل شود و سپس به طور عمده از انسانی به انسان دیگر منتقل شود. در آخرین مورد، پاتوژن جدید انسانی هنوز هم ممکن است از افراد به مخزن حیوانات منتقل شود، که در صورت تماس با حیوان، راهی دیگر برای انتقال به انسان است.
بنابراین، علاوه بر ایجاد مشکلات حفاظتی، به عنوان شکارچیان فرصت طلب حیوانات وحشی، گربه های اهلی ممکن است به آشکار ساختن پاتوژن های جعبه پاندورای حیات وحش (از جمله خفاش ها) با (الف) ابتلا به چنین عوامل بیماری زا از طریق طعمه های وحشی خود و انتقال آنها به انسان ها و (ب) فراهم آوردن یک محیط تکاملیبعدی که در نهایت ممکن است منجر به بیماریهایی شود که انسان هایا سایر حیوانات را مبتلا نماید،کمک کنند (شکل 2). علاوه بر این، گربه ها به دلیلکنش های متقابل فراوان و مکرر با مردم، معمولاً در تماس فیزیکی هستند، ممکن است میزبان عوامل بیماری زای انسانی باشند و این موارد را به خفاش ها منتقل نمایند (شکل 2).
خفاش ها به دلیل فیزیولوژی خاص و تاریخ طبیعی، بسیار مقاوم به ویروس ها هستند [46]، بنابراین در بدترین سناریوها، کنش متقابل توضیح داده شده در بالا ممکن است خفاش ها را به مخازن ویروسی عوامل بیماری زا تبدیل کند که در صورت عدم انتقال با میانجی شکارچی، هرگز به آنها به خفاش ها نخواهد رسید. آنها، علاوه بر اینکه گونه های حفاظت شده هستند که در اکثر کشورها به شدت محافظت می شوند (در اتحادیه اروپا، همه گونه های خفاش و زیستگاه آنها تحت دستورالعمل زیستگاه های43/92 محافظت می شوند)، خفاش ها خدمات مهم اکوسیستمی مانند حشره کشی، گرده افشانی و پراکندگی بذر را انجام می دهند [47، 48]، و سرکوب حشرات توسط خفاش ها در واقع یک دفاع طبیعی مهم در برابر بیماری های منتقله از راه بندپایان است. بنابراین، اگر خفاش ها به یک مخزن جدید پاتوژن تبدیل شوند، از بین بردن خفاش ها حتی در سناریوهای اضطراری فرضی نیز باید به عنوان یک راه حل منتفی شود، زیرا مطمئناً پیامدهای مخربی برای عملکرد اکوسیستم، اقتصاد انسان و سلامت به همراه خواهد داشت.
2. آخرین وضعیت تبادل پاتوژن ها بین خفاش - گربه
2.1 هاری
شناخته شده ترین بیماری که ممکن است از خفاش ها به گربه ها و در نهایت انسان منتقل شود هاری است، بیماری زئونوزی که باعث 590،000 مرگ انسان در سال می شود و بیش از 100 کشور جهان را تحت تأثیر قرار می دهد [49]. سرایت انسانی در اثر تماس با بزاق حیوان آلوده ایجاد می شود. موارد بیماری لاساویروس هاری (RABV) در آمریکا اغلب با خفاش ها مرتبط است [50،51]، و این ویروس نیز بطور مکرر از گربه های اهلی جدا شد. برای مثال، فقط در سال 2007 ، 8/3 درصدمواردRABV گزارش شده در ایالات متحده و پورتوریکو از گربه ها بودند (274 نفر= تعداد [52]). در همان منطقه جغرافیایی، در سال 2018، گربه ها 9/4درصداز 4951 موردبیماری هاری حیواناترا شامل می شود [53]. لاساویروس غیر از لاساویروس هاری مانند لاساویروس های خفاش اروپایی (EBLV)تیپ 2 و 3، همچنین به طور بالقوه برای افراد که هنوز در سراسر اروپا شیوع انسانی بسیار کمی دارند، کشنده هستند، خفاش ها به عنوان میزبان اصلی هستند و همچنین به ندرت از گربه های اهلی در قلمرو اروپا جدا شده اند [54] تماس بین گربه های اهلی و خفاش های هار اپتسیکوس سروتینوسدر هلند گزارش شده است [55]. به تازگی، گربه ای در ایتالیای مرکزی پس از گزیدن انسان مرد و آزمایش وی برای سایر لاساویروس، لاساویروس خفاش قفقاز غربی مثبت بود [49]،که قبلاً در مینی پتروس شریبرسی از جنوب شرقی اروپا [56] جدا شده بود - گونه ای مهاجر نیز در ایتالیا مشاهده می شود [57]. جدایه های ویروس آفریقایی موکولا (جنس لاساویروس) نیز در گربه های اهلی بازیابی می شود که ممکن است ناشی از شکار یک مخزن طبیعی خفاش یا جوندگان باشد [58].
اگرچه در بسیاری از موارد، گربه ها احتمالاً از سایر حیات وحشمانند گوشتخواران نیز آلوده می شوند، اما این تصویر هنوز هم خطر غیر قابل چشم پوشی از رویدادسرریز از خفاش ها به گربه هایاهلی را نشان می دهد [59]، که در واقع مشاهده شده است [60]. گرچه به نظر میرسد گربه ها در برابر ابتلا به هاری از طریق بلعیدن بافت آلوده مقاوم هستند [61]، آنها ممکن است هنگام گرفتن خفاش ها هنگام ظهور غروب از استراحتگاه، در معرض گزش خفاش (و از طریق آلوده شوند) قرار بگیرند. به دلیل تغییر حرکت و کاهش واکنش، یک خفاش هار افتاده روی زمین در اطراف محل استراحتگاه گله آنها[59] ممکن است برای شکارچی جذاب باشد [62،63]. در حالی که خطر گزش توسط یک گونه حیوان وحشی هار توسط انسان کم است [64]، اما وقتی صحبت از حیوانات اهلی مانند گربه ها می شود، این به طور شهودی و قابل ملاحظه بالاتر است. از این طریق، حتی مناطق بدون هاری از نظر تاریخی - به ویژه هنگامی که گونه های خفاش مهاجر را درگیر می کنند [65] - و محیط های شهری یا روستایی [66-68] ممکن است تحت تأثیر قرار گیرند. برای مثال، در برزیل، در سال های 2008 تا 2016، تنها 4/1درصد موارد گزش مردم توسط حیوانات مربوط به حیات وحش در مقابل 94درصدگزش توسط سگها و گربه ها بوده است [64]. در همان کشور، واریانت های ویروس های هاری که در جمعیت خفاش های خون آشام دسمودوس رویتاندوسدر گردش است نیز در گربه های خانگی جدا شده و از هر دو گونه حیوانی به انسان منتقل می شود [69]. علاوه بر این، هاری ممکن است به طور بالقوه از طریق خراش گربه ها به انسان منتقل شود، که آسیب های شایع مربوط به کنش متقابل مردم و گربه است [70]. بنابراین گربه های اهلی ممکن است یک مسیر جدید برای انتشار سرریز [71] باشد که از طریق آن یک برروز ناچیز انتقال هاری خفاش به انسان افزایش می یابد.
2.2. سایر بیماریها
علاوه بر هاری، طیف وسیعی از بیماری ها ممکن است به طور مستقیمیا غیرمستقیم گربه ها، خفاش ها و انسان ها را درگیرنماید. برای مثال، مشخص شده که گربه هایاهلی به ویروس هایحنیپاویروسو فیلوویروس ها جدا شده از خفاش ها حساس هستند و بنابراین ممکن است به عنوان میزبان واسطه در طغیان های این عوامل بیماری زا عمل کنند، اما در این مورد شکاف های مهم دانشی وجود دارد ([72]،در مطالعه مروری).ویروس های دیگر مانند اپتسیکوس فوکوس هرپسویروس (EfHV)، گاماهرپس ویروس ممکن است در سلولهای خفاش، گربه و انسان تکثیر شوند [73]. بعلاوه، انتقال بین گونه ها شامل خفاش ها، گربه ها و انسان ها ممکن است موجب بازآرایی ویرایش های ژنتیکی ویروس شود، که ممکن است در ویروس هایی که در حال حاضر برای انسان بیماری زا هستند، نیزاتفاق افتد [74].
باکتریهای گرم منفی از جنس پاستورلاهمزیست حفره های دهان سگها و گربه ها هستند و ممکن است گاهی اوقات از طریق گزش یا خراشیدن انسان را آلوده کنند [75] در این میان، گزارش شده که پاستورلا مولتوسیدا خفاشهای وسپرتیلیونید(ناهیدی) آزادزی را آلوده کرده و آنها را از بین میبرد، که معمولاً به وسیله سپتی سمی ناشی از پاستورلوز می میرند. شواهد قابل توجهی وجود دارد که سویه های پاستورلا مولتوسیدا با منشاء گربه پس از تلاش برای شکار گربه به خفاش ها منتقل شده اند [33]، بنابراین حتی خفاش هایی که از حمله جان سالم به در برده اند، ممکن است به عفونت زخم مبتلا شده و پس از آن بمیرند. سایر باکتری های منتقل شده به خفاش ها به همان روشی که ممکن است به این پستانداران نیز آسیب برساند، باکتری های خانواده انتروباکتریاسه است [33]. در میان تک یاخته ها، توکسوپلاسما گوندی، یک پاتوژن زئونوزی-گربه باعث ایجاد توکسوپلاسموز در انسان هایی که اغلب توسط گربه های اهلی به آنها منتقل می شود، (البته به ندرت) در خفاش ها مشاهده می شود، که شامل ژنوتیپ هایی است که قبلاً از گربه ها جدا شده اند [76،77]. سایر تک یاخته های مضر برای انسان مانند تریپانوزوما کروزی دارای مجموعه ای از مخازن وحشی و اهلی از جمله خفاش ها و گربه ها هستند [78]، با این وجود انتقال مستقیم بین این گونه ها ثبت نشده است. مخمرهایی که حیوانات و انسانها مبتلا می کنند مانند گونه های مالاسزیا، برخی از آنها باعث اختلالات پوستی در افراد می شوند، اغلب بر روی پوست و کانال شنوایی گربه ها و سگهای اهلی وجود دارد و همچنین در خفاش ها نیز تشخیص داده شده اند، که نشان دهنده فرضیه نوپدیدی مسیرهای زئونوزی است که این بار قارچ ها را شامل می شود [79].
انگل های خارجیبندپایان ناقلین شناخته شده ای هستند که بیماری ها را به میزبان خود منتقل می کنند و می توانند مستقیماً در رویدادهای سرریز نقش داشته باشند [80]. اگرچه این انگلها اغلب از اختصاصی میزبان هستند، برخی از آنها فرصت طلب می باشند، مانند کک گورکن (پاراسرا ملیس)، که در چندین پستاندار وحشی مشاهده می شود، اما همچنین در سگها، گربه ها، خفاش ها (رینولوفوس هیپوسیدروس) و انسانها نیز مشاهده می شود [81].
کک مورد بحث ناقل تریپانوزوما پستانیاست که گورکن های اروپایی را مبتلا می نماید [82]. به همین ترتیب، جرب ها مانند کانیس دمودکس ممکن است گربه ها و سگ ها و همچنین خفاش ها را آلوده به انگل نمایند [83] و به ندرت باعث دمودیکوز در انسان می شوند [84]. در چنین مواردی،انگل های خارجی بندپایان ممکن است یک ارتباط اپیدمیولوژیک بین میزبانهای مختلف ایجاد کرده و انسانها را از طریق گربه به خفاشها متصل نماید، اما این مسیر بالقوه بدون مطالعه است و تحقیق لازم دارد.
3. سارس-کووی-2و خطر انتقال انسان به خفاش. نقشی برای گربه ها؟
طی چند ماه گذشته، در مدت (در زمان نگارش) پاندمی غم انگیز که هنوز در حال انجام است، رسانه ها اغلب خفاش ها را به عنوان منبع اپیدمیولوژیکسارس-کووی-2، ویروس عامل کووید -19، ارائه می دهند، پستانداران در یک دید منفی و آنها را در معرض عواقب بالقوه حفاظت از قبیل کشتار عمدی و آشفتگی گله قرار دادند [85]. در واقع، خفاش های رینولوفید (خفاش نعلاسبی کوچک) از جنوب چین میزبان سایر کروناویروسها بودند (Bat CoV RaTG13 و RmYN02) که از نظر فیلوژنتیک کاملاً با سارس-کووی-2مرتبط هستند و این امر به منشاء مشترک این ویروس اشاره دارد [86]. اگرچه خفاش ها ناعادلانه به عنوان مقصر بیماری همه گیر نشان داده می شوند، اما دلایل واقعی آن را باید در شکار خفاش و تجارت برای مصرف انسان جستجو کرد [87]. اینکه آیا تکامل سارس-کووی-2ممکن است میزبانان دیگری مانند پانگولین (مورچه خوارهایپولکی) را درگیر کرده باشد [88] مشخص نیست و به تازگی مورد سئوال قرار گرفته است [89]، اما بدون شک بازارهای حیوانات زنده که خفاش ها، پنگولین ها و سایر حیوانات وحشی با هم و در آن نگهداری می شوند تماس نزدیک با مردم، ذبح و فروش درجا شرایط ایده آل برای نوپدیدی بیماریهای ویروسی جدید فراهم می کند [87]. اگرچه کووید -19یک بیماری انسانی است که منشاءزئونوزی دارد، تحقیقات نشان داد پروتئین های سنبله ایسارس-کووی-2ممکن است علاوه بر انسان به پروتئین هایACE2موجود در سطح سلول چندین پستاندار دیگر متصل شوند [90]. در حقیقت، مواردی از پستانداران غیر انسانی آلوده به سارس-کووی-2شامل ببرها و شیرهای اسیر، راسوهای آمریکایی در مراکز پرورشی و همچنین در طبیعت و حیوانات خانگی وجود داشته است (برای بررسی به [91] مراجعه نمائید). در مورد خفاش ها، این تصویر نامشخص است و به دور از بررسی جامع است. روزتوس اجیپتیاکوسممکن است به طور آزمایشی آلوده شود اما هیچ علائمی از خود نشان ندهد [92]، در حالی که سایر گونه ها، از جمله تاداریدا برازیلینسو رینولوفیدها، احتمالاً حساس به انتقال انسان به خفاش قرار دارند [91].
از طرف دیگر، خفاشهای بزرگ قهوه ایاپتسیکوس فوکوس که به آنهابه طور تجربیسارس-کووی-2 تلقیح شدند و در برابر عفونت مقاوم بودند [93]. به طور کلی، واکنش به ویروس می تواند کاملا اختصاصی- گونه ای باشد، که با توجه به غنای جهانی گونه های مختلف خفاش (بیش از 1400 گونه) و وقوع گسترده سارس-کووی-2در میان انسان ها، کمک چندانی نمی کند.
بر اساس تنوع بالای کروناویروس های موجود در خفاش ها و تمایل نشان داده شده توسط این عوامل بیماری زا برای تغییر میزبان [94]، نگرانی اصلی متخصصان حفاظت از محیط زیست این است که انتقال سارس-کووی-2از انسان به خفاش (یا سایر حیوانات وحشی) یک مخزن جدید در این پستانداران ایجاد کند که ممکن است امواج دیگری از عفونت از آن جرقه زده شود (شکل 2). اگر این اتفاق بیافتد، به وضوح یک مسئله مدیریتی بسیار چالش برانگیز و عواقب نامطلوب برای حفاظت از خفاش، به ویژه در مناطق شهری را تشکیل می دهد [91]. علاوه بر این، با گسترش در حیات وحش، از جمله خفاش ها، سارس-کووی-2ممکن است فرصتی برای تکامل و سازگاری با طیف وسیعی از میزبانهای جدید داشته باشد. بر این اساس، در سال 2020، کمیته مشورتی خفاش های اروپا بلافاصله توصیه هایی را درباره خطرات احتمالی انتقال سارس-کووی-2 از انسان به خفاش منتشر کرد (کمیته مشورتی خفاش های اروپا توافق نامه برنامه محیط زیست سازمان ملل متحد (UNEP) درباره حفاظت از جمعیت خفاش های اروپا است: در سایت زیر در 25 ژانویه 2021قابل دسترسی است). در همان سال، برای جلوگیری از چنین خطرات، اتحادیه بین المللی حفاظت از گروه خفاش طبیعتراهنمایی را با هدف طیف متنوعی از ذینفعان از جمله محققان خفاش، توانبخش ها، غارنوردان و بازدید کنندگان غارها و جمع آورندگان گوانو یا چلغوز صادر کرد از 25 ژانویه 2021 در سایت زیر، قابل دسترسی است.
بعید به نظر می رسد حضور خفاش های خانه نشیندر محل گله آنها در واقع خطر واقعی برای انتقال مستقیم سارس-کووی-2 از انسان به خفاش باشد؛ با این حال، به ویژه در زمینه های روستایی یا شهری، گربه های اهلی ممکن است از نظر فرضی فاصله فیزیکی افراد را از خفاش ها جدا کنند و از طریق شکار باعث گسترش ویروس به خفاش ها شوند. در واقع، افراد ممکن است سارس-کووی-2را به گربه هایی که حساس به ویروس هستند، منوط به انتقال کارآمد (همچنین از طریق هوا) ویروس منتقل نمایند، همانطور که از هر دو مورد ثبت شده و کارهای تجربی مشخص است [95–100]. اگرچه پیش بینی احتمال انتقال سارس-کووی-2 توسط گربه سانان دشوار است، اما بر اساس دانش کم موجود ناچیز به نظر می رسد، اما بدون تردید مسئله به دلیل پیامدهای قابل توجه آن از نظر خطر زئونوزی و پیامدهای حفاظت شایسته توجه کامل است.
4. جلوگیری از خطرات زئونوزی مرتبط با شکار خفاش توسط گربه ها: راهنمای تحقیق و مدیریت
از آنچه تاکنون نشان داده شده، باید روشن باشد که گربه هایاهلی نه تنها تهدیدی برای حفاظت از خفاش به وجود نمی آورند، بلکه نشان دهنده یک ارتباط اپیدمیولوژیکی بین انسان و خفاش است که در آن پاتوژن ها می توانند در هر دو جهت پخش شوند. بر این اساس، ما اصرار داریم که اقدامات مناسبی برای جلوگیری از خطر زئونوزی در ارتباط با گربه ها، به ویژه در مجاورت گلههای خفاش شناخته شده به شرح زیرانجام شود:
1- جمعیت گربه های اهلی باید بخشی از برنامه هایمراقبت فعال با هدف شناسایی حضور احتمالی عوامل بیماری زا باشد که ممکن است در زنجیره انتقال انسان- خفاش-گربه نقش داشته باشد. این برنامه باید گربه هایی را که در فضای باز رها شده اند، هدف قرار دهد، که نه تنها شامل گربه های ولگردمی شود بلکه گربه های صاحب دار پرسه زنی- آزاد نیز هستند.
2. در کشورهایی مانند ایتالیا، گربه های پرسه زن- آزاد در شهر که در کلنی ها زندگی می کنند توسط قانون محافظت می شوند. این گربه ها حق زندگی آزاد را به رسمیت می شناسند، نه کشته می شوند و نه جابجا می شوند، توسط خدمات دامپزشکی مقامات بهداشت محلی عقیم می شوند و توسط مراقبان رسمی و سازمانی گربه ها مراقبت می شوند [101]. در حالی که این درجه حفاظت مطمئناً شرایط گربه های ولگرد را بهبود بخشیده و اهداف مهم رفاه حیوانات را دنبال کرده، عواقب آن از نظر تأثیر بر تنوع زیستی حیوانات شهری ناشناخته و نادیده گرفته شده است. ما پیشنهاد می کنیم که این کلنی ها از نظر تأثیرات آنها بر حیات وحش، و خفاش های خاص تر، به طور سیستماتیک کنترل شوند و نتایج احتمالی زئونوزی برای توسعه استراتژی های مدیریت مناسب ارزیابی شود. برای کلنی های گربه که باید در مکان هایی که معلوم است یک گله خفاش وجود دارد اقدامات ویژه ای نیز باید انجام شود.
3- گربه های فضای باز باید به عنوان یک عامل تهدید در تمام برنامه های حفاظت با هدف مدیریت کلنی های شناخته شده خفاش در نظر گرفته شوند، و اقدامات لازم، از جمله اقدامات قانونی، برای جلوگیری از تماس بین گربه ها و خفاش ها انجام شود.
4- در صورت لزوم، بایدپویش های واکسیناسیون گربه هایی که در فضای باز زندگی می کنند، برای کاهش خطرات عمده زئونوزی از جمله موارد مرتبط با هاری تقویت شود و تحقیقات بیشتر لازم است انجام شود، تا ببینید آیا واکسن های دامپزشکی غیرفعال هاری موجود در بازار، که از سویه هایRABV تهیه شده اند، می توانند از گربه ها در برابر لاساویروس های مختلف که در اروپا گردش می کنند، بطور متقاطع حفاظت کنند [102]. خطر توقف پویش های واکسیناسیون در مناطقی که به تازگی بدون هاری اعلام شده، نیز باید ارزیابی شود [103].
5- شکار گربه در حیات وحش یک فرایند پیچیده است که ریشه عمیقی در تاریخ تکامل گربه ها دارد اما به طیف وسیعی از متغیرها از جمله نیازهای غذایی و صفات فیزیولوژیکی، تاریخچه زندگی اولیه، شخصیت فردی و عوامل محیطی بستگی دارد [104]. درک بهتر از وزن نسبی این متغیرها برای ایجاد استراتژی های مناسب برای جلوگیری از شکار گربه ها در حیات وحش و خفاش ها به طور خاص مهم است، و کار خاص باید در مورد کنش های متقابل خفاش - گربه انجام شود، از جمله مواردی که شامل خفاش های بیمار است. برای مثال، در مطالعه ای درباره روند مکانی- زمانی در بیماری هاری خفاش در ایالت واشنگتن که خطر مرتبط زئونوزی را ارزیابی می کند، گربه ها تقریباً 90 درصد خفاشهای اسیر شده توسط حیواناتاهلی را گرفتند، اما سگ ها بیشتر خفاش های هار را صید می کنند [105]. الگوهایی از این دست به وضوح با خصوصیات رفتاری شکار گربه در ارتباط است و درک آنها به جلوگیری یا کاهش خطرات زئونوزی کمک می کند. مطالعات سیستماتیک شکار گربه روی خفاش ها باید علاوه بر مشاهدات رفتاری، ارزیابی مولکولی رژیم غذایی گربه ها و همکاری دقیق با مراکز توان بخشی حیات وحش، جایی که خفاش های آسیب دیده توسط گربه ها اغلب پذیرفته می شوند [13]. با اطمینان از اینکه یک خفاش کشته شده یا زخمی شده توسط گربه است، امروز به لطف تکنیک های تجزیه و تحلیل DNA پزشکی قانونی امکان پذیر است، که حتی می تواند برای ارتباط وقایع شکار با گربه های منفرد استفاده شود [32] و اجازه بازرسی از شکارچیان و طعمه ها را برای حضور بالقوه، یا انتقال عوامل بیماری زا می دهد. برآورد میزان بقاء در میان خفاش ها به دنبال تلاش برای شکار از گربه ها نیز برای ارزیابی بهتر خطر بالقوه زئونوزی مرتبط با اینرویدادها کلیدی است.
6- از آنجا که ابزارهایی برای کشف سناریوهای اپیدمیولوژیک در دسترس است [106]، از جمله استفاده از سامانه اطلاعات جغرافیایی (GIS)و مدل سازی فضایی، برنامه های کاربردی برای موقعیت یابی مردم، گربه ها و خفاش ها در مناطق روستایی و شهری مورد نیاز است.
7- گربه های اهلی بسیار محبوب هستند و بسیاری از مردم، از جمله دوستداران حیوانات با حسن نیت، گربه ها را در فضای باز نگه می دارند تا نیاز "استقلال و آزادی" حیوان اهلی خود را برآورده کنند. تأثیر گربه بر حیات وحش اغلب به عمد مورد توجه قرار می گیرد، باعث ایجاد خصومت در بین عاشقان گربه می شود و حتی گاهی اوقات توسط "رمز سکوت" واقعی تشدید می شود. با این حال، شواهد فزاینده ای وجود دارد که نشان می دهد شکار حیات وحش توسط گربه ها (برای مثال ، [9،14،28])، از جمله خفاش ها ([107]؛ این مطالعه) تا حد زیادی دست کم گرفته می شود. برای تشویق مردم به نگهداری از گربه در خانه بایدپویش های آگاهی بخشی انجام شود، که در واقع نه تنها حیات وحش را از شکار محافظت می کند، بلکه گربه ها را از بسیاری از خطرات ناشی از زندگی در محیط خارج و افراد در برابر خطرات زئونوزی که در مورد آنها بحث کردیم، محافظت می کند.
8- سرانجام، محققان در این مقاله بر همکاری بیشتری بین ذینفعان بالقوه (متخصصان حفاظت از محیط زیست، سازمان های رفاه حیوانات، مقامات بهداشت انسانی، ویروس شناسان و غیره) برای اجرای استراتژی های مناسب سلامت واحد و جلوگیری یا حداقل کاهش اثر خطرات انتقال عوامل بیماری زا از خفاش-گربه- انسانی تاکید دارند.
References
1. Bengis, R.G.; Leighton, F.A.; Fischer, J.R.; Artois, M.; Morner, T.; Tate, C.M. The role of wildlife in emerging and re-emerging zoonoses. Rev. Sci. Tech. 2004, 23, 497–512.
2. Huong, N.Q.; Nga, N.T.; Long, N.V.; Luu, B.D.; Latinne, A.; Pruvot, M.; Phuong, N.T.; Quang, L.T.; Hung, V.V.; Lan, N.T.; et al. Coronavirus testing indicates transmission risk increases along wildlife supply chains for human consumption in Vietnam, 2013–2014. PLoS ONE 2004, 15, e0237129.
3. Arora, N.K.; Mishra, J. COVID-19 and importance of environmental sustainability. Environ. Sustain. 020, 3, 117–119. [CrossRef]
4. Cui, J.A.; Chen, F.; Fan, S. Effect of intermediate hosts on emerging zoonoses. Vector Borne Zoonotic Dis. 2017, 17, 599–609. [CrossRef]
5.Nor, M.M.; Gan, C.H.; Ong, B.L. Nipah virus infection of pigs in peninsular Malaysia. Rev. Sci. Tech.2000, 19, 160–165.
6. Hayman, D.T.S.; Bowen, R.A.; Cryan, P.M.; McCracken, G.F.; O’shea, T.J.; Peel, A.J.; Gilbert, A.; Webb, C.T.; Wood, J.L.N. Ecology of zoonotic infectious diseases in bats: Current knowledge and future directions. Zoonoses Public Health 2013, 60, 2–21. [CrossRef]
7. Mollentze, N.; Streicker, D.G. Viral zoonotic risk is homogenous among taxonomic orders of mammalian and avian reservoir hosts. Proc. Natl. Acad. Sci. USA 2020, 117, 9423–9430. [CrossRef]
8. López-Baucells, A.; Rocha, R.; Fernández-Llamazares, Á. When bats go viral: Negative framings in virological research imperil bat conservation. Mamm. Rev. 2018, 48, 62–66. [CrossRef]
9. Woolley, L.A.; Geyle, H.M.; Murphy, B.P.; Legge, S.M.; Palmer, R.; Dickman, C.R.; Augusteyn, J.; Comer, S.; Doherty, T.S.; Eager, C.; et al. Introduced cats Felis catus eating a continental fauna: Inventory and traits of Australian mammal species killed. Mamm. Rev. 2019, 49, 354–368. [CrossRef]
10.Capizzi, D. A review of mammal eradications on Mediterranean islands. Mamm. Rev. 2020, 50, 124–135. [CrossRef]
11.Marra, P.; Santella, C. Cat Wars: The Devastating Consequences of a Cuddly Killer; Princeton University Press: Princeton, NJ, USA;Oxford, UK, 2016; p. 223.
12. Li, Y.; Wan, Y.; Shen, H.; Loss, S.R.; Marra, P.P.; Li, Z. Estimates of wildlife killed by free-ranging cats in China. Biol. Conserv. 2021, 253, 108929. [CrossRef]
13. Ancillotto, L.; Serangeli, M.T.; Russo, D. Curiosity killed the bat: Domestic cats as bat predators. Mamm. Biol. 2013, 78, 369–373.[CrossRef]
14. Mori, E.; Menchetti, M.; Camporesi, A.; Cavigioli, L.; Tabarelli de Fatis, K.; Girardello, M. Licence to kill? Domestic cats affect a wide range of native fauna in a highly biodiverse Mediterranean country. Front. Ecol. Evol. 2019, 7, 477. [CrossRef]
15.Woinarski, J.C.; South, S.L.; Drummond, P.; Johnston, G.R.; Nankivell, A. The diet of the feral cat (Felis catus), red fox (Vulpes vulpes) and dog (Canis familiaris) over a three-year period at Witchelina Reserve, in arid South Australia. Aust. Mammal. 2018, 40, 204–213.[CrossRef]
16. Holden, C.; Mutze, G. Impact of rabbit haemorrhagic disease on introduced predators in the Flinders Ranges, South Australia.Wildl. Res. 2002, 29, 615–626. [CrossRef]
17. Romano, M.C.; Maidagan, J.I.; Pire, F.E. Behavior and demography in an urban colony of Tadaridabrasiliensis (Chiroptera:Molossidae) in Rosario, Argentina. Rev. Biol. Trop. 1999, 47, 1121–1127. [CrossRef]
18.Rodríguez-Durán, A.; Pérez, J.; Montalbán, M.A.; Sandoval, J.M. Predation by free-roaming cats on an insular population of bats.ActaChiropt. 2010, 12, 359–362. [CrossRef]
19.Scrimgeour, J.; Beath, A.; Swanney, M. Cat predation of short-tailed bats (Mystacinatuberculatarhyocobia) in rangataua forest, Mount Ruapehu, central North Island, New Zealand. N. Z. J. Zool. 2012, 39, 257–260. [CrossRef]
20.Daniel, M.J.; Williams, G.R. A survey of the distribution, seasonal activity and roost sites of New Zealand bats. N. Z. J. Ecol. 1984, 7, 9–25.
21. Borroto-Páez, R.; Mancina, C.A. Biodiversity and conservation of Cuban mammals: Past, present, and invasive species. J. Mammal. 2017, 98, 964–985. [CrossRef]
22. da Costa-Pinto, A.L. First record of natural predation on bats by domestic cat in Brazil, with distribution extension for Phyllostomus discolor. Oecol. Aust. 2020, 24, 242–248. [CrossRef]
23.Bigai, L.R.; Faria, M.B. Eventospredatóriosemmorcegos no Brasil. Rev. Biol. Neotrop. 2018, 15, 96–108. [CrossRef]
24. Delpietro, H.; Konolsaisen, F.; Marchevsky, N.; Russo, G. Domestic cat predation on vampire bats (Desmodusrotundus) while foraging on goats, pigs, cows and human beings. Appl. Anim. Behav. Sci. 1994, 39, 141–150. [CrossRef]
25.Mancina, C.A. Phyllonycterispoeyi (Chiroptera: Phyllostomidae). Mamm. Species 2010, 42, 41–48. [CrossRef]
26. Vincenot, C.E.; Koyama, L.; Russo, D. Near threatened? First report of unsuspected human-driven decline factors in the Ryukyu flying fox (Pteropusdasymallus) in Japan. Mamm. Biol. 2015, 80, 273–277. [CrossRef]
27. Tidemann, C.R.; Yorkston, H.D.; Russack, A.J. The diet of cats, Felis catus, on Christmas Island, Indian ocean. Wildl. Res. 1994, 21, 279–285.[CrossRef]
28.Palmas, P.; Jourdan, H.; Rigault, F.; Debar, L.; De Meringo, H.; Bourguet, E.; Mathiveta, M.; Leea, M.; Adjouhgniopea, R.; Papillona, Y.; et al. Feral cats threaten the outstanding endemic fauna of the NewCaledonia biodiversity hotspot. Biol. Conserv. 2017, 214, 250–259. [CrossRef]
29. Brickner-Braun, I.; Geffen, E.; Yom-Tov, Y. The domestic cat as a predator of Israeli wildlife. Isr. J. Ecol. Evol. 2007, 53, 129–142.CrossRef]
30. Phillips, S.; Coburn, D.; James, R. An observation of cat predation upon an eastern blossom bat Syconycteris australis. Aust. Mammal. 2001, 23, 57–58. [CrossRef]
31.Kutt, A.S. The diet of the feral cat (Felis catus) in north-eastern Australia. Acta Theriol. 2011, 56, 157–169. [CrossRef]
32. Khayat, R.O.S.; Grant, R.A.; Ryan, H.; Melling, L.M.; Dougill, G.; Killick, D.R.; Shaw, K.J. Investigating cat predation as the cause of bat wing tears using forensic DNA analysis. Ecol. Evol. 2020, 20, 8368–8378. [CrossRef]
33.Mühldorfer, K.; Speck, S.; Wibbelt, G. Diseases in free-ranging bats from Germany. BMC Vet. Res. 2011, 7, 61. [CrossRef]
34. Vázquez-Domínguez, E.; Ceballos, G.; Cruzado, J. Extirpation of an insular subspecies by a single introduced cat: The case of the endemic deer mouse Peromyscus guardia on Estanque Island, Mexico. Oryx 2004, 38, 347–350. [CrossRef]
35. Vlaschenko, A.; Kovalov, V.; Hukov, V.; Kravchenko, K.; Rodenko, O. An example of ecological traps for bats in the urban environment. Eur. J. Wildl. Res. 2019, 65, 20. [CrossRef]
36. Calver, M.; Thomas, S.; Bradley, S.; McCutcheon, H. Reducing the rate of predation on wildlife by pet cats: The efficacy and practicability of collar-mounted pounce protectors. Biol. Conserv. 2007, 137, 341–348. [CrossRef]
37. Hall, C.M.; Fontaine, J.B.; Bryant, K.A.; Calver, M.C. Assessing the effectiveness of the Birdsbesafe
® anti-predation collar cover in reducing predation on wildlife by pet cats in Western Australia. Appl. Anim. Behav. Sci. 2015, 173, 40–51. [CrossRef]
38. Triggs, B.; Brunner, H.; Cullen, J.M. The food of fox, dog and cat in Croajingalong National Park, south-eastern Victoria. Wildl. Res. 1984, 11, 491–499. [CrossRef]
39. Jones, E.; Coman, B.J. Ecology of the feral cat, Felis catus (L.), in south-eastern Australia I. Diet. Wildl. Res. 1981, 8, 537–547.[CrossRef]
40. Read, J.L.; Dagg, E.; Moseby, K.E. Prey selectivity by feral cats at central Australian rock-wallaby colonies. Aust. Mammal. 2019, 41, 132–141.[CrossRef]
41. Rismiller, P.D.; McKelvey, M.W. Twenty-seven years of wildcats and kittens, case history of a feral predator on the Pelican Lagoon Peninsula, Kangaroo Island. In Feral Cat Control, Some New Ideas for 2003, Kangaroo Island/Roxby Downs; Kangaroo Island Rotary Club: Kingscote, Australia, 2003; pp. 9–16.
42.Virkar, P.S.; Shrotriya, S. Threat to wildlife from carnivorous pets: A case of cat attacking Indian Pipistrelle Pipistrellus coromandra (Gray, 1838). Zoo’s Print 2013, 28, 25–27.
43. Rocha, R. Look what the cat dragged in: Felis silvestriscatus as predators of insular bats and instance of predation on the endangered Pipistrellus maderensis. Barb 2015, 8, 18–21.
44. Khayat, R.O.S.; Shaw, K.J.; Dougill, G.; Melling, L.M.; Ferris, G.R.; Cooper, G.; Grant, R.A. Characterizing wing tears in common pipistrelles (Pipistrellus pipistrellus): Investigating tear distribution, wing strength, and possible causes. J. Mammal. 2019, 100, 1282–1294. [CrossRef] [PubMed]
45. Miller, B.; Mullette, K.J. Rehabilitation of an endangered Australian bird: The Lord Howe Island woodhen Tricholimnas sylvestris (Sclater). Biol. Conserv. 1985, 34, 55–95. [CrossRef]
46.Hayman, D.T. Bat tolerance to viral infections. Nat. Microbiol. 2019, 4, 728–729. [CrossRef]
47. Kunz, T.H.; Braun de Torrez, E.; Bauer, D.; Lobova, T.; Fleming, T.H. Ecosystem services provided by bats. Ann. N. Y. Acad. Sci. 2011, 1223, 1–38. [CrossRef]
48. Russo, D.; Bosso, L.; Ancillotto, L. Novel perspectives on bat insectivory highlight the value of this ecosystem service in farmland: Research frontiers and management implications. Agric. Ecosyst. Environ. 2018, 266, 31–38. [CrossRef]
49. Gossner, C.M.; Mailles, A.; Aznar, I.; Dimina, E.; Echevarría, J.E.; Feruglio, S.L.; Lange, H.; Maraglino, F.P.; Parodi, P.;Perevoscikovs, J.; et al. Prevention of human rabies: A challenge for the European Union and the European Economic Area.Eurosurveillance 2020, 25, 2000158. [CrossRef]
50. World Health Organization (WHO). WHO Expert Consultation on Rabies: Third Report; WHO: Geneva, Switzerland, 2018. Available online:https://apps.who.int/iris/handle/10665/272364(accessed on 25 January 2021).
51. Velasco-Villa, A.; Orciari, L.A.; Juárez-Islas, V.; Gómez-Sierra, M.; Padilla-Medina, I.; Flisser, A.; Souza, V.; Castillo, A.; Franka, R.; Escalante-Mañe, M.; et al. Molecular diversity of rabies viruses associated with bats in Mexico and other countries of the Americas. J. Clin. Microbiol. 2006, 44, 1697–1710. [CrossRef]
52. Blanton, J.D.; Palmer, D.; Christian, K.A.; Rupprecht, C.E. Rabies surveillance in the United States during 2008. J. Am. Vet. Med. Assoc. 2009, 235, 676–689. [CrossRef]
53. Ma, X.; Monroe, B.P.; Cleaton, J.M.; Orciari, L.A.; Gigante, C.M.; Kirby, J.D.; Chipman, R.B.; Fehlner-Gardiner, C.; Gutiérrez Cedillo, V.; Petersen, B.W.; et al. Public Veterinary Medicine: Public Health: Rabies surveillance in the United States during 2018. J. Am. Vet. Med. Assoc. 2020, 256, 195–208. [CrossRef]
54. Dacheux, L.; Larrous, F.; Mailles, A.; Boisseleau, D.; Delmas, O.; Biron, C.; Bouchier, C.; Capek, I.; Muller, M.; Ilari, F.; et al. European bat lyssavirus transmission among cats, Europe. Emerg. Infect. Dis. 2009, 15, 280. [CrossRef]
55. Takumi, K.; Lina, P.H.C.; Van der Poel, W.H.M.; Kramps, J.A.; Van Der Giessen, J.W.B. Public health risk analysis of European bat lyssavirus infection in The Netherlands. Epidemiol. Infect. 2009, 137, 803–809. [CrossRef] [PubMed]
56.Botvinkin, A.D.; Poleschuk, E.M.; Kuzmin, I.V.; Borisova, T.I.; Gazaryan, S.V.; Yager, P.; Rupprecht, C.E. Novel lyssaviruses isolated from bats in Russia. Emerg. Infect. Dis. 2003, 9, 1623–1625. [CrossRef]
57. Wright, P.G.; Newton, J.; Agnelli, P.; Budinski, I.; Di Salvo, I.; Flaquer, C.; Fulco, A.; Georgiakakis, P.; Martinoli, A.; Mas, M.; et al. Hydrogen isotopes reveal evidence of migration of Miniopterusschreibersii in Europe. BMC Ecol. 2020, 20, 1–7. [CrossRef]
58. Sabeta, C.; Blumberg, L.; Miyen, J.; Mohale, D.; Shumba, W.; Wandeler, A. Mokola virus involved in a human contact (South Africa). FEMS Immunol. Med. Microbiol. 2010, 58, 85–90. [CrossRef]
59. Shankar, V.; Orciari, L.A.; Mattos, C.D.; Kuzmin, I.V.; Pape, W.J.; O’Shea, T.J.; Rupprecht, C.E. Genetic divergence of rabies viruses from bat species of Colorado, USA. Vector Borne Zoonotic Dis. 2005, 5, 330–341. [CrossRef]
60. Jaramillo-Reyna, E.; Almazán-Marín, C.; de la O-Cavazos, M.E.; Valdéz-Leal, R.; Bañuelos-Álvarez, A.H.; Zúñiga-Ramos, M.A.; Melo-Munguía, M.; Gómez-Sierra, M.; Sandoval-Borja, A.; Chávez-López, S.; et al. Public Veterinary Medicine: Public Health Rabies virus variants identified in Nuevo Leon State, Mexico, from 2008 to 2015. J. Am. Vet. Med. Assoc. 2020, 256, 438–443.[CrossRef]
61. Shirakawa, R.K.; Cortez, A.; Richtzenhain, L.J.; Itoou, T.; Sakai, T.; Ito, F.H. Ensaiossobreinoculação intramuscular e alimentação de gatosdomésticos (Felis catus) com cérebros de camundongospréviamenteinoculados com vírus da raiva. Braz. J. Vet. Res. Anim. Sci. 2007, 44, 125–133. [CrossRef]
62. Genaro, G. Gatodoméstico: Futurodesafio para controle da raivaemáreasurbanas? Pesqui. Vet. Bras. 2010, 30, 186–189.[CrossRef]
63. Ribeiro, J.; Staudacher, C.; Martins, C.M.; Ullmann, L.S.; Ferreira, F.; Araujo, J.P.; Biondo, A.W. Bat rabies surveillance and risk factors for rabies spillover in an urban area of Southern Brazil. BMC Vet. Res. 2018, 14, 1–8. [CrossRef]
64. Benavides, J.A.; Megid, J.; Campos, A.; Hampson, K. Using surveillance of animal bite patients to decipher potential risks of rabies exposure from domestic animals and wildlife in Brazil. Front. Public Health 2020, 8, 318. [CrossRef] [PubMed]
65. Morikawa, V.M.; Ribeiro, J.; Biondo, A.W.; Fellini, A.; Bier, D.; Molento, M.B. Cat infected by a variant of bat rabies virus in a29-year disease-free urban area of southern Brazil. Rev. Soc. Bras. Med. Trop. 2012, 45, 255–256. [CrossRef]
66. Miranda, A.O.; Núñez, S.E.; Martinez, L.; Gury–Dohmen, D.M. Molecular analysis of urban rabies case from vampire bat inCorrientes, Argentina. Rev. Vet. 2009, 20, 77–80. [CrossRef]
67. Castilho, J.G.; De Souza, D.N.; Oliveira, R.N.; Carnieli, P., Jr.; Batista, H.B.C.R.; Pereira, P.M.C.; Achkar, S.M.; Macedo, C.I. Theepidemiological importance of bats in the transmission of rabies to dogs and cats in the state of São Paulo, Brazil, between 2005and 2014. Zoonoses Public Health 2017, 64, 423–430. [CrossRef]
68. BannazadehBaghi, H.; Alinezhad, F.; Kuzmin, I.; Rupprecht, C.E. A Perspective on Rabies in the Middle East—Beyond Neglect.Vet. Sci. 2018, 5, 67. [CrossRef]
69. Araújo, I.L.; Oliveira, T.M.; Diniz, S.A.; Silva, M.X. Análiseepidemiológica dos atendimentos da profilaxiaantirrábicahumanaassociadosaacidentes com gatos. Arq. Bras. Med. Vet. Zootec. 2020, 72, 814–822. [CrossRef]
70. Wang, X.; Werner, B.G.; Konomi, R.; Hennigan, D.; Fadden, D.; Caten, E.; Soliva, S.; DeMaria, A. Animalrabies in Massachusetts,1985–2006. J. Wildl. Dis. 2009, 45, 375–387. [CrossRef] [PubMed]
71.Teng, C.H.E.N.; Miao, F.M.; Ye, L.I.U.; Zhang, S.F.; Zhang, F.; Nan, L.I.; Hu, R.L. Possible transmission of irkut virus from dogs tohumans. Biomed. Environ. Sci. 2018, 31, 146–148.
72.Glennon, E.E.; Restif, O.; Sbarbaro, S.R.; Garnier, R.; Cunningham, A.A.; Suu-Ire, R.D.; Osei-Amponsah, R.; Wood, J.L.N.; Peel, A.J.Domesticated animals as hosts of henipaviruses and filoviruses: A systematic review. Vet. J. 2018, 233, 25–34. [CrossRef]
73.Subudhi, S.; Rapin, N.; Dorville, N.; Hill, J.E.; Town, J.; Willis, C.K.; Bollinger, T.K.; Misra, V. Isolation, characterization andprevalence of a novel Gammaherpesvirus in Eptesicus fuscus, the North American big brown bat. Virology 2018, 516, 227–238.
[CrossRef]
74.Okitsu, S.; Hikita, T.; Thongprachum, A.; Khamrin, P.; Takanashi, S.; Hayakawa, S.; Maneekarn, N.; Ushijima, H. Detection andmolecular characterization of two rare G8P[14] and G3P[3] rotavirus strains collected from children with acute gastroenteritis inJapan. Infect. Genet. Evol. 2018, 62, 95–108. [CrossRef]
75. Westling, K.; Farra, A.; Cars, B.; Ekblom, A.G.; Sandstedt, K.; Settergren, B.; Wretlind, B.; Jorup, C. Cat bite wound infections:A prospective clinical and microbiological study at three emergency wards in Stockholm, Sweden. J. Infect. 2006, 53, 403–407.[CrossRef] [PubMed]
76. Fournier, G.F.D.S.R.; Lopes, M.G.; Marcili, A.; Ramirez, D.G.; Acosta, I.C.L.; Ferreira, J.I.G.D.S.; Cabral, A.; Lima, J.T.R.D.; Pena, H.;Dias, R.; et al. Toxoplasma gondii in domestic and wild animals from forest fragments of the municipality of Natal, northeasternBrazil. Rev. Bras. Parasitol. Vet. 2014, 23, 501–508. [CrossRef] [PubMed]
77.Cabral, A.D.; Gama, A.R.; Sodré, M.M.; Savani, E.S.M.M.; Galvão-Dias, M.A.; Jordão, L.R.; Maeda, M.M.; Yai, L.E.O.; Gennari, S.M.;Pena, H.F.J. First isolation and genotyping of Toxoplasma gondii from bats (Mammalia: Chiroptera). Vet. Parasitol. 2013, 193, 100–104.[CrossRef] [PubMed]
78. Wehrendt, D.P.; Gómez-Bravo, A.; Ramirez, J.C.; Cura, C.; Pech-May, A.; Ramsey, J.M.; Abril, M.; Guhl, F.; Schijman, A.G.Development and evaluation of a duplex TaqMan qPCR assay for detection and quantification of Trypanosoma cruzi infection indomestic and sylvatic reservoir hosts. Parasit. Vectors 2019, 12, 1–9. [CrossRef] [PubMed]
79. Gandra, R.F.; Gambale, W.; Simao, R.D.C.G.; da Silva Ruiz, L.; Durigon, E.L.; de Camargo, L.M.A.; Giudice, M.C.;Sanfilippo, L.F.; de Araújo, J.; Paula, C.R. Malassezia spp. in acoustic meatus of bats (Molossus molossus) of the AmazonRegion, Brazil. Mycopathologia 2008, 165, 21–26. [CrossRef]
80.Marshall, A.G. The Ecology of Ectoparasitic Insects; Academic Press Inc.: London, UK, 1981; p. 446.
81.Ancillotto, L.; Mazza, G.; Menchetti, M.; Mori, E. Host specificity of the badger’s flea (Paracerasmelis) and first detection on a bathost. Parasitol. Res. 2014, 113, 3909–3912. [CrossRef]
82. Lizundia, R.; Newman, C.; Buesching, C.D.; Ngugi, D.; Blake, D.; Sin, Y.W.; Macdonald, D.W.; Wilson, A.; McKeever, D. Evidencefor a role of the host-specific flea (Paracerasmelis) in the transmission of Trypanosoma (Megatrypanum) pestanai to the Europeanbadger. PLoS ONE 2011, 6, e16977. [CrossRef]
83.Sastre, N.; Francino, O.; Curti, J.N.; Armenta, T.C.; Fraser, D.L.; Kelly, R.M.; Hunt, E.; Silbermayr, K.; Zewe, C.; Sánchez, A.; et al.Detection, prevalence and phylogenetic relationships of Demodex spp and further skin prostigmata mites (Acari, Arachnida) inwild and domestic mammals. PLoS ONE 2016, 11, e0165765. [CrossRef]
84.Dik, B. A dog related Demodex spp. infestation in a student: A rare Demodex case. Mikrobiyol Bul. 2018, 52, 214–220.
85. Rocha, R.; Aziz, S.A.; Brook, C.E.; Carvalho, W.D.; Cooper-Bohannon, R. Bat conservation and zoonotic disease risk: A researchagenda to prevent misguided persecution in the aftermath of COVID-19. Anim. Conserv. 2020. [CrossRef]
86. Zhou, H.; Chen, X.; Hu, T.; Li, J.; Song, H.; Liu, Y.; Wang, P.; Liu, D.; Yang, J.; Holmes, E.C.; et al. A novel bat coronavirus closelyrelated to SARS-CoV-2 contains natural insertions at the S1/S2 cleavage site of the spike protein. Curr. Biol. 2020, 30, 2196–2203.[CrossRef] [PubMed]
87. Aguirre, A.A.; Catherina, R.; Frye, H.; Shelley, L. Illicit wildlife trade, wet markets, and COVID-19: Preventing future pandemics.World Med. Health Policy 2020, 12, 256–265. [CrossRef] [PubMed]
88. Zhang, T.; Qunfu, W.; Zhigang, Z. Probable pangolin origin of SARS-CoV-2 associated with the COVID-19 outbreak. Curr. Biol.2020, 30, 1346–1351. [CrossRef] [PubMed]
89. Frutos, R.; Serra-Cobo, J.; Chen, T.; Devaux, C.A. COVID-19: Time to exonerate the pangolin from the transmission of SARS-CoV-2to humans. Infect. Genet. Evol. 2020, 84, 104493. [CrossRef]
90. Wan, Y.; Shang, J.; Graham, R.; Baric, R.S.; Li, F. Receptor recognition by the novel coronavirus from Wuhan: An analysis basedon decade-long structural studies of SARS coronavirus. J. Virol. 2020, 94, e00127-20. [CrossRef]
91. Gryseels, S.; De Bruyn, L.; Gyselings, R.; Calvignac-Spencer, S.; Leendertz, F.H.; Leirs, H. Risk of human-to-wildlife transmissionof SARS-CoV-2. Mamm. Rev. 2020. [CrossRef]
92. Schlottau, K.; Rissmann, M.; Graaf, A.; Schön, J.; Sehl, J.; Wylezich, C.; Höper, D.; Mettenleiter, D.C.; Balkema-Buschmann, A.;Harder, T.; et al. SARS-CoV-2 in fruit bats, ferrets, pigs, and chickens: An experimental transmission study. Lancet Microbe2020, 1, 218–225. [CrossRef]
93. Hall, J.S.; Knowles, S.; Nashold, S.W.; Ip, H.S.; Leon, A.E.; Rocke, T.; Keller, S.; Carossino, M.; Balasuriya, D.; Hofmeister, E.Experimental challenge of a North American bat species, big brown bat (Eptesicus fuscus), with SARS-CoV-2. TransboundEmerg.Dis. 2020. [CrossRef]
94. Colunga-Salas, P.; Hernández-Canchola, G. Bats and humans during the SARS-CoV-2 outbreak: The case of bat-coronavirusesfrom Mexico. TransboundEmerg. Dis. 2020. [CrossRef]
95. Sailleau, C.; Dumarest, M.; Vanhomwegen, J.; Delaplace, M.; Caro, V.; Kwasiborski, A.; Hourdel, V.; Chevaillier, P.; Barbarino, A.;Comtet, L.; et al. First detection and genome sequencing of SARS-CoV-2 in an infected cat in France. TransboundEmerg. Dis.2020, 1–5. [CrossRef]
96.MANFQ. Update Corona BijDieren. Ministry of Agriculture, Nature and Food Quality of the Netherlands. 2020. Available online:https://www.rijksoverheid.nl/documenten/kamerstukken/2020/05/15/kamerbrief-over-corona-bij-dieren(accessed on 25January 2021).
97.USDA. Confirmed Cases of SARS-CoV-2 in Animals in the United States. Animal and Plant Health Inspection Service of theUnited States Department of Agriculture. 2020. Available online:https://www.aphis.usda.gov/aphis/ourfocus/animalhealth/sa_one_health/sars-cov-2-animals-us(accessed on 25 January 2021).
98. AFCD. Pet Cat Tests Positive for COVID-19. Agriculture Fisheries and Conservation Department of theHong Kong Special AdministrativeRegion. 2020. Available online:https://www.news.gov.hk/eng/2020/03/20200331(accessed on 25 January 2021).
99. FASFC. Zoönotischrisico van het SARS-CoV2 Virus (Covid-19) bijGezelschapsdieren: Infectie van diernaarmensen vanmensnaardier; Federal Agency for the Safety of the Food Chain: Brussels, Belgium, 2020. Available online:http:
//www.afsca.be/wetenschappelijkcomite/adviezen/2020/_documents/Spoedraadgeving04-2020_SciCom2020-07_Covid-19gezelschapdieren_27-03-20.pdf(accessed on 25 January 2021).
100.Newman, A.; Smith, D.; Ghai, R.R.; Wallace, R.M.; Torchetti, M.K.; Loiacono, C.; Murrell, L.S.; Carpenter, A.; Moroff, S.; Rooney, J.A.; et al.First reported cases of SARS-CoV-2 infection in companion animals—New York, March–April 2020. MMWR Morb. Mortal. Wkl.Rep. 2020, 69, 710–713. [CrossRef]
101. Natoli, E.; Malandrucco, L.; Minati, L.; Verzichi, S.; Perino, R.; Longo, L.; Pontecorvo, F.; Faini, A. Evaluation of Unowned
Domestic Cat Management in the Urban Environment of Rome After 30 Years of Implementation of the No-Kill Policy (Nationaland Regional Laws). Front. Vet. Sci. 2019, 6, 31. [CrossRef]
102. Servat, A.; Wasniewski, M.; Cliquet, F. Cross-Protection of Inactivated Rabies Vaccines for Veterinary Use against Bat LyssavirusesOccurring in Europe. Viruses 2019, 11, 936. [CrossRef]
103.Dias, R.A.; Rocha, F.; Ulloa-Stanojlovic, F.M.; Nitsche, A.; Castagna, C.; de Lucca, T.; Rodrigues, R.C.A. Spatiotemporaldistribution of a non-haematophagous bat community and rabies virus circulation: A proposal for urban rabies surveillance inBrazil. Epidemiol. Infect. 2019, 147, e130. [CrossRef]
104. Cecchetti, M.; Crowley, S.L.; McDonald, R.A. Drivers and facilitators of hunting behaviour in domestic cats and options formanagement. Mamm. Rev. 2020. [CrossRef]
105. Bonwitt, J.; Oltean, H.; Lang, M.; Kelly, R.M.; Goldoft, M. Bat rabies in Washington State: Temporaspatial trends and risk factorsfor zoonotic transmission (2000–2017). PLoS ONE 2018, 13, e0205069. [CrossRef] [PubMed]
106.Arias Caicedo, M.R.; Xavier, D.D.A.; Arias Caicedo, C.A.; Andrade, E.; Abel, I. Epidemiological scenarios for human rabiesexposure notified in Colombia during ten years: A challenge to implement surveillance actions with a differential approach onvulnerable populations. PLoS ONE 2019, 14, e0213120. [CrossRef] [PubMed]
107. Oedin, M.; Brescia, F.; Millon, A.; Murphy, B.P.; Palmas, P.; Woinarski, J.C.Z.; Vidal, E. Cats Felis catusas a threat to bats worldwide:A review of the evidence. Mamm. Rev. 2021. [CrossRef]











 تشکر و قدردانی از دکتر میرزمانی بزرگوار بابت ترجمه این مقاله جالب و مفید.
تشکر و قدردانی از دکتر میرزمانی بزرگوار بابت ترجمه این مقاله جالب و مفید. 








مفید بود . ممنون از جناب دکتر میرزمانی