اپیدمیولوژی آنفلوانزای آسیب رسان فوق حاد طیور ویروس A(H5N8)
دكتر علی صفر ماکنعلی
متخصص اپيدميولوژی بيماريهای قابل انتقال دامی
مشاور بين المللی سابق سازمان خواربار كشاورزی ملل متحد در كنترل بيماريهای فرامرزی
مشاور بين المللی سابق اتحاديه اروپا براي برنامه های توسعه ای بهداشت دام
مقدمه:
در سطح کشورهای عضو اتحادیه ی اروپا، مصوبات شورای اتحادیه ی اروپا بعنوان اسناد بالا دستی برای دیده وری، کنترل، پیشگیری و ریشه کنی بیماری آنفلوانزای آسیب رسان فوق حاد مورد استفاده قرار می گیرند و هیچ کشوری از کشورهای عضو اتحادیه ی اروپا فراتر از این مصوبات اقدام دیگری را انجام نمی دهد. وزن افرادی که در تهیه و تدوین این برنامه ها فعالیت می کنند، بسیار بالا و از افرادی که مبنای انتخاب آنها تخصص و مهمتر از همه تجربه میدانی می باشد، صورت می پذیرد.
اقدامات لازم در سطح کشورهای عضو اتحادیه ی اروپا برای ردیابی و کنترل ویروس های آنفلوانزای آسیب رسان فوق حاد بر اساس محورهای زیر می باشد:
1. مصوبه شورای اتحادیه اروپا برای دیده وری در طیور اهلی
2. مصوبه شورای اتحادیه اروپا برای دیده وری در پرندگان وحشی
3. مصوبه شورای اتحادیه اروپا در رابطه با اعمال معیار های کنترلی
4. مصوبه شورای اتحادیه اروپا برای تشخیص آنفلوانزای پرندگان
در کشورهای عضو اتحادیه اروپا گروهی از افراد مسئولیت تجزیه و تحلیل سریع رخداد ها را به عهده دارند و گزارشات آنها بر روی وب سایت اتحادیه اروپا منتشر می شود که آخرین گزارش تجزیه و تحلیل آنها در رابطه با ویروس های جدید A(H5N8) در تاریخ 18 نوامبر (28 آبان 1395) منتشر شده است.
در کنار این موضوع، گزارشات مراجع ذیصلاح کشورهای عضو اتحادیه اروپا در رابطه با همه بیماری ها از جمله بیماری آنقلوانزای آسیب رسان فوق حاد در یک روند زمانی و در قالب جدول زمانی خاص منتشر می گردد؛ لذا با توجه به تماس بعضی از مدیران کل دامپزشکی استان ها در رابطه با ورود، پخش و سایر موضوعات اپیدمیولوژیکی مرتبط با این بیماری، در این قسمت به موضوعات اپیدمیولوژیکی مرتبط با این بیماری و گزارشی مختصر بر روند آن در کشور هلند پرداخته می شود به امید اینکه مورد استفاده همکاران و سایر بهره برداران قرار گیرد.
اپیدمیولوژی ویروس A(H5N8)
در سال میلادی جاری برای اولین بار در تاریخ 27 اکتبر 2016 میلادی (پنج شنبه، 6 آبان 1395) مرجع ذیصلاح بهداشت دام کشور مجارستان رخداد ویروس های جدید A(H5N8) را در یک قطعه قو وحشی گزارش داد و تا تاریخ 18 نوامبر سال میلادی جاری (جمعه، 28 آبان 1395) نیز در کشور های اتریش، مجارستان و آلمان این ویروس هم در پرندگان وحشی و هم در طیور بومی گزارش شده است؛ ولی کشورهای کرواسی، دانمارک، لهستان و سوییس صرفاً بیماری را در پرندگان وحشی گزارش داده اند.
برای اولین بار ویروس های A(H5N8) در سال 2010 میلادی در بین پرندگان وحشی در آسیا در کشورهایی مانند چین، ژاپن و کره جنوبی شناسایی و جداسازی شد و باعث بروز رخدادهایی در طیور صنعتی گردید و در سال 2016 میلادی نیز برای دومین بار از طریق مهاجرت بهاره پرندگان وحشی وارد اروپا شد که در مقایسه با سال 2014-2015 میلادی میزان مرگ و میر حاصل از آن در پرندگان افزایش یافته است. آنالیزهای ژنتیکی اولیه حکایت از آن دارد که این ویروس ها از نظر ژنتیکی مرتبط با ویروس های سال 2014-2015 می باشد، اما ویروس های جدید A(H5N8) یک خوشه جدید متفاوتی را تشکیل داده اند.
روش های مراقبت و نظارت در پرندگان وحشی مهاجر و مقیم و طیور اهلی، معدوم سازی پرندگان آلوده و اعمال برنامه های خاص امنیت زیستی در سطح کشورهای عضو اتحادیه ی اروپا نقش بسیار مهمی در مهار ویروس داشته است. از دیدگاه بهداشت عمومی تا حال حاضر موردی از آلودگی انسان به ویروس های جدید A(H5N8) گزارش نشده است و بر اساس ارزیابی مخاطرات احتمالی انجام گرفته، خطر احتمالی آن برای جمعیت انسانی بسیار پایین می باشد. البته علیرغم اینکه بر اساس آنالیز ژنومی انجام گرفته مبنی بر اینکه این ویروس ها اساساً مختص پرندگان می باشند، ولی خطر احتمالی آن برای انسان قابل اغماض نمی باشد و معیارهای محافظتی خاص برای جلوگیری از عفونت انسانی باید بشدت به خصوص توسط کسانی که تماس مستقیم با پرندگان دارند، رعایت شود؛ همچنین افرادی که در معرض آلودگی با این ویروس قرار گرفته اند، باید به مدت 10 روز برای بروز و یا عدم بروز تب و علائم آنفلوانزا تحت نظر باشند و مراجع ذیصلاح بهداشتی انسانی، درمان های پیشگیرانه برای افرادی که در معرض ویروس H5N1 انجام می شد را برای افرادی که در معرض ویروس A(H5N8) قرار می گیرند را نیز توصیه می کنند. در کشورهای عضو اتحادیه اروپا به کسانی که شغل آنها کار با پرندگان و طیور می باشد، توصیه شده است که از واکسن آنفلوانزای فصلی قبل از شروع فصل سرما استفاده کنند.
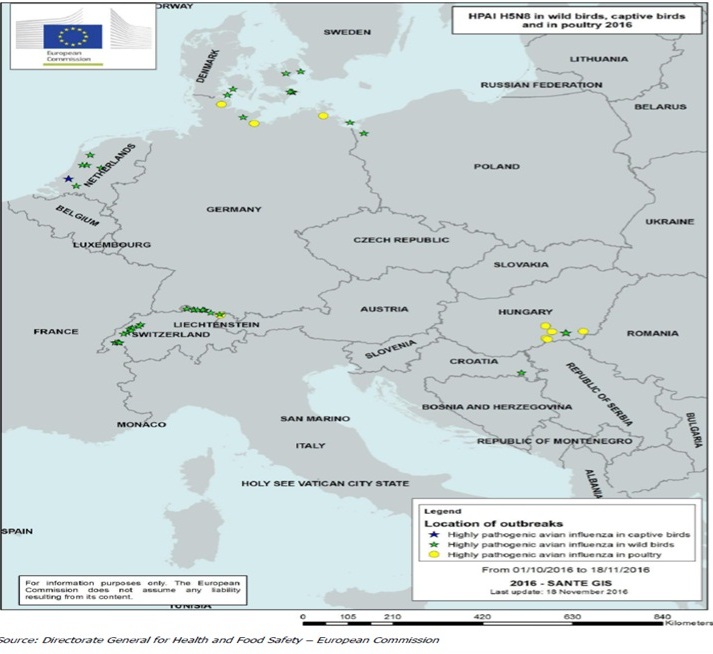
نقشه ی A(H5N8) در اروپا ( 28/ آبان/95)
نقشه ی زیر مناطقی از اروپا را که در آنها ویروس های جدید در پرندگان وحشی، پرندگان در اسارت و طیور بومی شناسایی شده است را نشان می دهد
میزان ابتلا و مرگ و میر پرندگان در اثر ابتلا به ویروس های A(H5N8)
بر اساس گزارشات رسمی منتشر شده در کشور هایی که بیماری را گزارش داده اند میزان ابتلا[5] در طیور تخمگذار بین 0.04 تا 25 درصد، میزان مرگ و میر[6] حدود 0.04 تا 25 درصد می باشد و میزان مرگ ومیر در طیور مبتلا[7] تقریباً 100 درصد می باشد. در بعضی از کشورها در طیور صعنتی میزان ابتلا و مرگ و میر تا 20 درصد هم در طیور گزارش شده است.
تابلوی بالینی طیور صنعتی شباهت هایی با بیماری نیوکاسل دارد. میزان ابتلا و مرگ و میر همیشه بصورت کلاسیک رخ لذا اجرای الگوریتم آزمایشگاهی برای تفریق سریع دو بیماری نیوکاسل و تیپ A آنفلوانزا بسیار حائز اهمیت می باشد. در برنامه های کشور های در حال توسعه و توسعه یافته از جمله در سطح کشورهای عضو اتحادیه ی اروپا برای نمونه های اخذ شده از موارد مشکوک به آنفلوانزای آسیب رسان فوق حاد، الگوریتم آزمایشگاهی مدونی وجود دارد که مورد استفاده قرار می گیرد.
مسیرهایی انتقال ویروس های A(H5N8) که از طریق پرندگان مهاجر وارد قاره ی اروپا می شوند
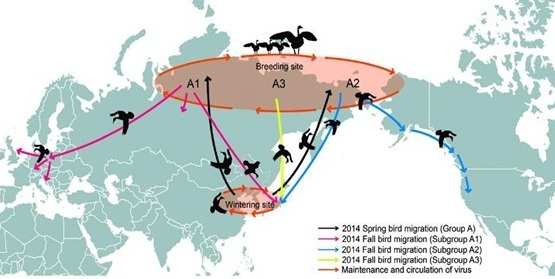
در نقشه زیر مسیرهای مهاجرت پرندگان نشان شده است (نقشه اقتباس شده از مجله ویروس شناسی سال 2015 میلادی می باشد)
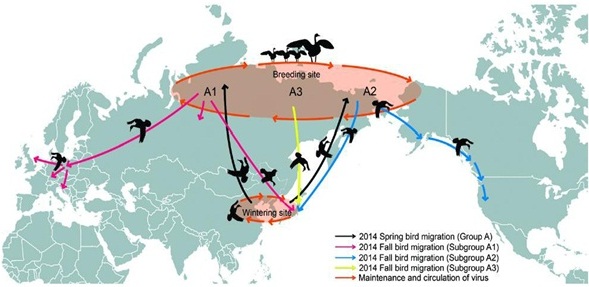
در این نقشه مسیرها به چهار دسته تقسیم شده است:
1. گروه A شامل کشورهای چین، روسیه، کره جنوبی، ژاپن که دارای ویروس های European and North American A(H5N8) 2.3.4.4 viruses می باشند
2. تحت گروه A1 شامل ویروس های H5N8اواخر سال 2014 میلادی اروپا و روسیه می باشند و تعداد سه ویروس از این دسته در ماه دسامبر سال 2014 میلادی در کشور ژاپن شناسایی شدند.
3. تحت گروه A2 شامل H5N8 و H5کلد 2.3.44 می باشند که حاصل تغییرات در ویروس های (A(H5N2) و A(H5N1) می باشند که در اواخر سال 2014 میلادی در آمریکای شمالی می باشند و یک ویروس ژاپنی A/crane/Kagoshima/KU1/2014(H5N8) در نوامبر 2014 شناسایی شدند.
4. تحت گروه A3 شامل ویروس های H5N8 می باشند که در ماه دسامبر 2014 میلادی و در ماه ژانویه 2015 میلادی در کره جنوبی شناسایی شدند.
تجزیه و تحلیل اطلاعات حاصل از مطالعات میدانی انجام گرفته حکایت از آن دارد که پرندگان وحشی احتمالاً منشاء ورود ویروس به قاره ی اروپا می باشند؛ پرندگان مهاجر آلوده که در فصل پاییز از مسیر شمال شرق به جنوب غرب از آسیا و روسیه به اروپا بر گشته اند، ویروس را با خود به اروپا آورده اند. در ماه مه سال 2015 میلادی (اردیبهشت ماه سال 1394) ویروس A(H5N8) در یک قوی وحشی در کشور روسیه در مسیر مهاجرت بین شرق آسیا و اروپا شناسایی شد. سازمان خواربار و کشاورزی ملل متحد (FAO) هم اعلام کرده است که پرندگان وحشی احتمالاً می توانند در گسترش ویروس در مسافت های طولانی از مسیر آسیا به اروپا نقش داشته باشند.
از آنجایی که ویروس HPAI A(H5N8) از مدفوع پرندگان وحشی در محیط دفع می شوند، انتقال ویروس از پرندگان وحشی مهاجر به پرندگان بومی می تواند به روش مستقیم و غیر مستفیم صورت پذیرد. واحد های طیور بومی آلوده در اروپا واحد هایی بوده اند که در مجاورت زیستگاه های پرندگان مهاجر بوده اند، یعنی در زیستگاههایی که لاشه پرندگان وحشی مهاجر مرده آلوده در آن یافت شده است، لذا اعمال سیستم غیر فعال آنفلوانزای فوق حاد طیور برای پرندگان خاص در زیستگاههای پرندگان مهاجر اولویت دارتر از انجام پایش های فعال هزینه بر، بی هدف و بدون نتیجه می باشد.
در گذشته ویروس های HPAI A(H5N8) باعث مرگ و میر بالا در اردک نمی شد این در حالی است که در سال میلادی 2016 مرگ و میر بالایی در پرندگان وحشی مهاجر را ویروس HPAI A(H5N8) باعث شده است، یعنی شدت بیماری زایی ویروس جدید افزایش یافته است. این ویروس علاوه بر طیور برای چندین گونه پرنده ی دیگر بشدت بیماری زا می باشد، ولی هنوز مشخص نیست که کدام پرنده می تواند ویروس را بدون اینکه علائم و عوارضی را نشان دهد با خود جابجا کند، یعنی مشخص نشده است که کدام پرنده نفش حامل را دارد .
جلوگیری از تماس طیور بومی با پرندگان وحشی و افزایش سطح امنیت زیستی واحد های طیور مهمترین معیارهای پیشگیرانه برای جلوگیری از ورود ویروس به داخل واحد های طیور صنعتی می باشد و در صورت عدم ارتقاء سطح امنیت زیستی واحدهای مرغداری صنعتی بخصوص واحد هایی همانند طیور صنعتی تخم گذار که مدت زمان مواجهه و فاکتورهای خطرات احتمالی مواجهه آنها با ویروس بیشتر از سایر واحدها می باشند، به احتمال بسیار بسیار زیاد درگیر بیماری خواهند شد و کشور و مرغداران متحمل خسارات بسیار سنگین خواهند شد.
در صورتی که سطح امنیت زیستی واحد های طیور صنعتی ارتقاء نیابد، انجام هر پایشی در کشوری مانند ایران که دروازه های ورود ویروس در آن بسیار زیاد و گسترده می باشد، امری بیهوده و عبث بوده و خواهد بود. انجام سیستم دیده وری غیر فعال تشدیدی که بایستی حداقل یک ماه قبل از تغییر فصل شروع می شد، برای شناسایی هر گونه تغییرات معنی دار در مصرف آب و غذا و تلفات و علائم بالینی طیور صنعتی و عکس العمل سریع برای شناسایی ویروس در پرندگان وحشی و طیور روستایی، مهمترین روش برای جلوگیری از پخش ویروس و محافظت طیور صنعتی در برابر این ویروس به شمار می رود.
رخداد های ویروس های A(H5N8) در کشور هلند
ساختار جمعیت دامی در کشور هلند
در کشور هلند تعداد 2068 فارم صنعتی طیور وجود دارد. برای آشنایی بیشتر با وضعیت دام در کشور هلند، در جدول زیر ساختار جمعیت دامی در آورده شده است:
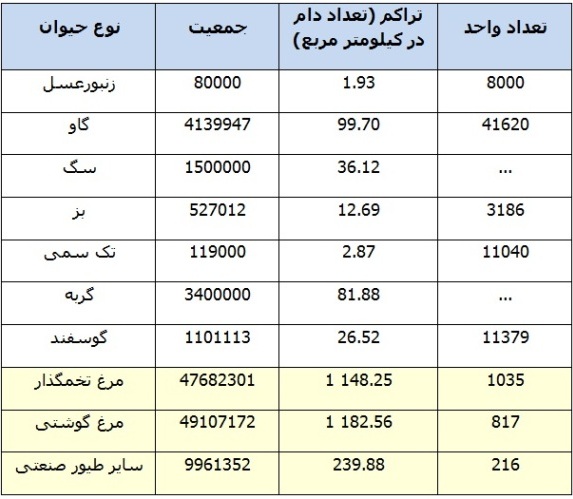
روند زمانی آنفلوانزای آسیب رسان فوق حاد طیور در کشور هلند در جدول زیر آمده است:
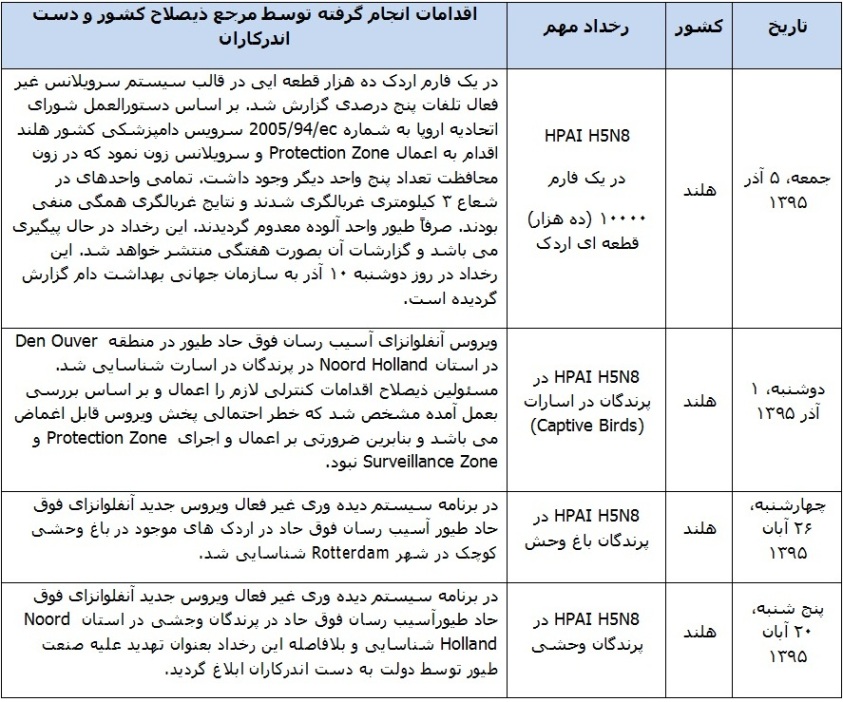
نتیجه گیری:
اعمال سیستم های دیده وری فعال، غیر فعال، تشدیدی و سانتینل در طیور اهلی، طیور صنعتی و پرندگان وحشی خاص به صورت هدفمند، اعمال معیارهای امنیت زیستی، اطلاع رسانی و مشارکت با دست اندرکاران کلیدی زنجیره ی طیور، حذف و معدوم سازی واحدهای آلوده نقش بسیار مهمی در مهار ویروس دارد.
در کشورهایی که سیستم دیده وری غیر فعال با پوشش جغرافیایی کامل داشته باشند، بدون نیاز به سیستم دیده وری فعال که وقت و هزینه ی بسیار بالایی را در بر دارد، می توان بطور موثری واحدهای صنعتی طیور و سایر جمعیت های حساس را در برابر مواجهه با ویروس بطور قابل قبولی محافظت نمود. معنی و مفهوم آن این است که سیستم دیده وری فعال زمانی لازم و از اهمیت خاص خود می تواند برخوردار باشد که قبل از آن به عنوان اولویت اول سیستم دیده وری غیر فعالی وجود داشته باشد که تمامی مناطق پرخطر و واحدهای طیور حساس و سایر پرندگان حساس را بر مبنای خطرات احتمالی پوشش داده باشد. در صورت عدم وجود سیستم دیده وری غیرفعال کامل، انجام سیستم دیده وری فعال کاری عبث ، بیهوده و گمره کننده می باشد و نتایج آن نمی تواند بعنوان Early Warning System در یک کشور و یا منطقه عمل کند.
در رابطه با پرندگان وحشی مهاجر و نقش آن ها در اپیدمیولوژی بیماری آنفلوانزای فوق حاد طیور، تحقیقات گسترده و عمیقی صورت پذیرفته که همگی بر این موضوع دلالت دارند که آنها می توانند باعث ورود ویروس به یک کشور یا منطقه بشوند، اما پخش آن ها در داخل یک کشور و یا یک منطقه توسط عوامل دیگر صورت می پذیرد. تعداد و سطح جغرافیایی درگیری واحد های طیور بومی و صنعتی در یک منطقه و یا یک کشور نشان دهنده این موضوع می تواند باشد که برنامه ی ملی کنترل بیماری آن کشور یا به درستی تهیه نشده است و یا اینکه به درستی اجرا نشده است.
منابع:
1. Wu H, Peng X, Xu L, Jin C, Cheng L, Lu X, et al. Novel reassortant influenza A(H5N8) viruses in domestic ducks, eastern China. Emerg Infect Dis. 2014 Aug;20(8):1315-8.
2. Lee YJ, Kang HM, Lee EK, Song BM, Jeong J, Kwon YK, et al. Novel reassortant influenza A(H5N8) viruses, South Korea, 2014. Emerg Infect Dis. 2014 Jun;20(6):1087-9.
3. Ku KB, Park EH, Yum J, Kim JA, Oh SK, Seo SH. Highly pathogenic avian influenza A(H5N8) virus from waterfowl, South Korea, 2014. Emerg Infect Dis. 2014 Sep;20(9):1587-8.
4. Jeong J, Kang HM, Lee EK, Song BM, Kwon YK, Kim HR, et al. Highly pathogenic avian influenza virus (H5N8) in domestic poultry and its relationship with migratory birds in South Korea during 2014. Vet Microbiol. 2014 Oct 10;173(3-4):249-57.
5. Fan S, Zhou L, Wu D, Gao X, Pei E, Wang T, et al. A novel highly pathogenic H5N8 avian influenza virus isolated from a wild duck in China. Influenza Other Respir Viruses. 2014 Nov 1.
6. Zhao K, Gu M, Zhong L, Duan Z, Zhang Y, Zhu Y, et al. Characterization of three H5N5 and one H5N8 highly pathogenic avian influenza viruses in China. Vet Microbiol. 2013 May 3;163(3-4):351-7.
7. World Organisation for Animal Health (OIE). Update on highly pathogenic avian influenza in animals (type H5 and H7) 2014 [15 Dec 2014].
8. Poen MJ, Verhagen JH, Manvell RJ, Brown I, Bestebroer TM, van der Vliet S, et al. Lack of virological and serological evidence for continued circulation of highly pathogenic avian influenza H5N8 virus in wild birds in the Netherlands, 14 November 2014 to 31 January 2016. Euro Surveill. 2016 Sep 22;21(38).
9. Kang HM, Lee EK, Song BM, Jeong J, Choi JG, Jeong J, et al. Novel reassortant influenza A(H5N8) viruses among domestic and wild ducks, South Korea, 2014. Emerg Infect Dis. 2015 Feb.
10. Kang HM, Lee EK, Song BM, Jeong J, Choi JG, Jeong J, et al. Novel reassortant influenza A(H5N8) viruses among inoculated domestic and wild ducks, South Korea, 2014. Emerg Infect Dis. 2015 Feb;21(2):298-304.
11. Verhagen JH, van der Jeugd HP, Nolet BA, Slaterus R, Kharitonov SP, de Vries PP, et al. Wild bird surveillance around outbreaks of highly pathogenic avian influenza A(H5N8) virus in the Netherlands, 2014, within the context of global flyways. Euro Surveill. 2015 Mar 26;20(12).
12. World Organisation for Animal Health (OIE). Terrestrial Animal Health Code (2014) [19 Nov 2014].
13. Kim Y-I, Pascua PNQ, Kwon H-I, Lim G-J, Kim E-H, Yoon S-W, et al. Pathobiological features of a novel, highly pathogenic avian influenza A(H5N8) virus. Emerg Microbes Infect.
14. Hanna A, Banks J, Marston DA, Ellis RJ, Brookes SM, Brown IH. Genetic Characterization of Highly Pathogenic Avian Influenza (H5N8) Virus from Domestic Ducks, England, November 2014. Emerg Infect Dis. 2015 May;21(5):879-82.
15. Pulit-Penaloza JA, Sun X, Creager HM, Zeng H, Belser JA, Maines TR, et al. Pathogenesis and transmission of novel HPAI H5N2 and H5N8 avian influenza viruses in ferrets and mice. Journal of Virology. 2015 July 29, 2015.
16. Richard M, Herfst S, van den Brand JM, Lexmond P, Bestebroer TM, Rimmelzwaan GF, et al. Low Virulence and Lack of Airborne Transmission of the Dutch Highly Pathogenic Avian Influenza Virus H5N8 in Ferrets. PLoS One. 2015;10(6):e0129827.
17. Food And Agriculture Organization of the United Nations (FAO). H5N8 highly pathogenic avian influenza (HPAI) of clade 2.3.4.4 detected through surveillance of wild migratory birds in the Tyva Republic, the Russian Federation – potential for international spread 2016 [11/11/2016].
18. Si Y, Wang T, Skidmore AK, de Boer WF, Li L, Prins HHT. Environmental Factors Influencing the Spread of the Highly Pathogenic Avian Influenza H5N1 Virus in wild birds in Europe. Ecology and Society. 2010;15(3).











 از دوست گرامی جناب آقای دکتر ماکنعلی تقاضا دارم این مطالعات را در خصوص مناطق مختلف پرورش طیور در سطح جهانی از جمله آمریکای شمالی، آمریکای مرکزی و کاراییب، آمریکای جنوبی، اروپای مرکزی و غربی، آسیای جنوب شرقی، .... ادامه دهند تا در نهایت مجموعه این مطالعات به صورت Inter-regional Comparative Epidemiology برای علاقمندان و دست اندرکاران قابل استفاده باشد.
از دوست گرامی جناب آقای دکتر ماکنعلی تقاضا دارم این مطالعات را در خصوص مناطق مختلف پرورش طیور در سطح جهانی از جمله آمریکای شمالی، آمریکای مرکزی و کاراییب، آمریکای جنوبی، اروپای مرکزی و غربی، آسیای جنوب شرقی، .... ادامه دهند تا در نهایت مجموعه این مطالعات به صورت Inter-regional Comparative Epidemiology برای علاقمندان و دست اندرکاران قابل استفاده باشد. 











@حکیم مهر یک پیشنهاد داشتم، لطفا ایمیل ایشان را به صورت تصویر درج فرمایید تا در مقابل اسپم ایمیلشان حفاظت شود.